4月10日,国家药品监督管理局官网显示,百济神州“替雷利珠单抗”新适应症已完成审批,用于治疗局部晚期或转移性尿路上皮癌(UC),继2019年12月获批复发或难治性经典型霍奇金淋巴瘤 (R/RcHL) 之后,替雷利珠单抗在国内成功获批第二个适应症,也将成为国内首款治疗尿路上皮癌的PD-1单抗。
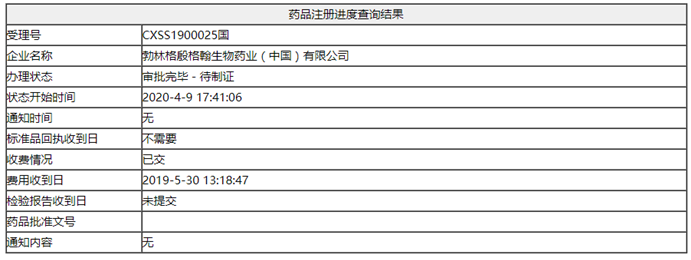
替雷利珠单抗是百济神州自主研发的一款PD-1单抗,于2019年12月被国家药监局批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(R/RcHL)患者,商品名为百泽安。百泽安是2019年新《药品管理法》生效后国内首个上市许可持有人采用委托生产模式获得上市批准的创新生物药,由勃林格殷格翰位于上海的生物制药生产基地生产。
此次替雷利珠单抗治疗UC的上市申请是基于一项关键II期临床研究(CTR20170071)结果,该研究共入组113例先前接受过治疗的、PD-L1呈阳性的局部晚期或转移性中国和韩国UC患者,中位随访时间为8个月。研究结果显示:替雷利珠单抗单药二线治疗UC的总缓解率(ORR)为23.1%,其中完全缓解率(CR)为7.7%,部分缓解率(PR)为15.4%。
除了用于治疗霍奇金淋巴瘤和尿路上皮癌,替雷利珠单抗还被开发用于治疗肺癌、肝癌、食管鳞状细胞癌、胃癌等高发癌种,且其一线鳞状NSCLC患者的sNDA有望于今年在国内递交。
目前,国内共有6款PD-1单抗获批,其中4款国产、2款进口。除了替雷利珠单抗,纳武利尤单抗治疗UC处于III临床阶段,特瑞普利单抗处于II临床研究阶段。(人民日报健康客户端 王月明整理)
(责任编辑:李宁)









网友评论