健康时报记者乔靖芳
如同出生医学证明是婴儿的有效法律凭证一样,药品说明书是是上市后药品使用的依据,非常重要。
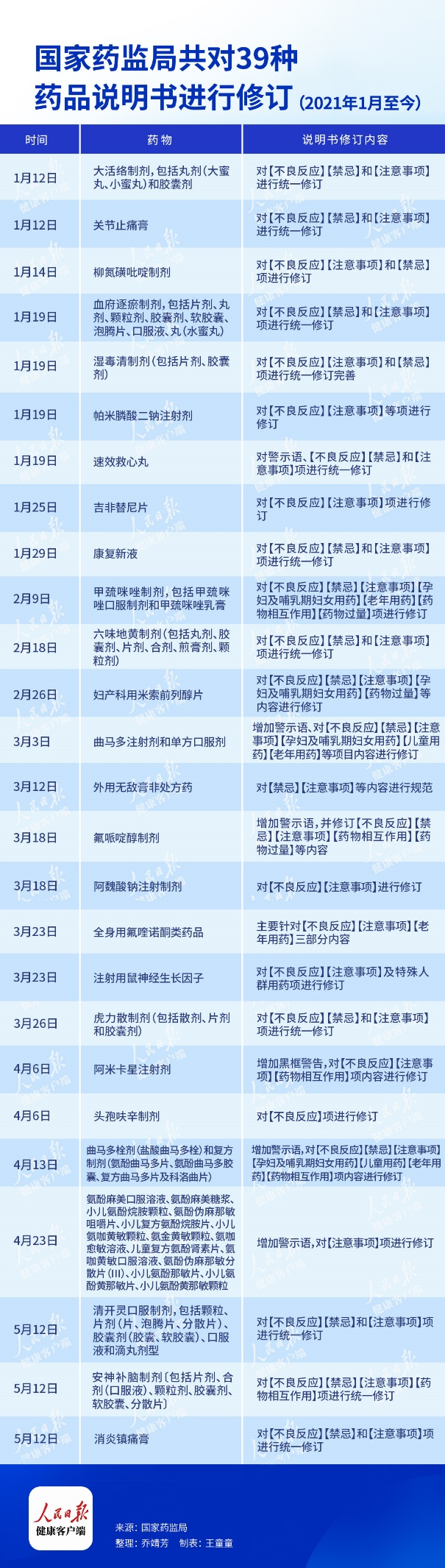
据健康时报统计发现,2021年1月至今,国家药监局共对39种药品说明书进行修订,其中一月份9种,二月份3种,三月份7种,四月份17种(仅4月23日就有14个品种),5月1日到5月15日3种。修订内容大多为增加警示语、对【不良反应】【禁忌】和【注意事项】等进行修订。
药品上市后为何还会修改药品说明书?
国家药监局官网曾发文解释:药品说明书主要包含药品安全性、有效性的重要科学数据、结论和信息,用以指导安全、合理使用药品。药品说明书应当充分包含药品不良反应信息,详细注明药品不良反应。由于药品在上市前的安全性研究中存在客观的局限性,在药品上市前临床研究过程中,受到许多客观因素限制,例如,病例少、研究时间短、试验对象年龄范围窄、用药条件控制较严等。因此,药品不良反应发现上存在时滞现象,这也决定了药品说明书的修改是动态的、不断完善的。药品生产企业应根据药品上市后的安全性、有效性情况及时修改说明书,国家药品监督管理部门也可以根据药品不良反应监测、药品再评价结果等信息要求药品生产企业修改药品说明书。












