5月6日,中国国家药品监督管理局(NMPA)官网公示,豪洛捷Aptima®HIV核酸检测试剂盒(RT-TMA法)获得批准,可用于体外定量和定性检测人血浆和血清中的病毒核酸。
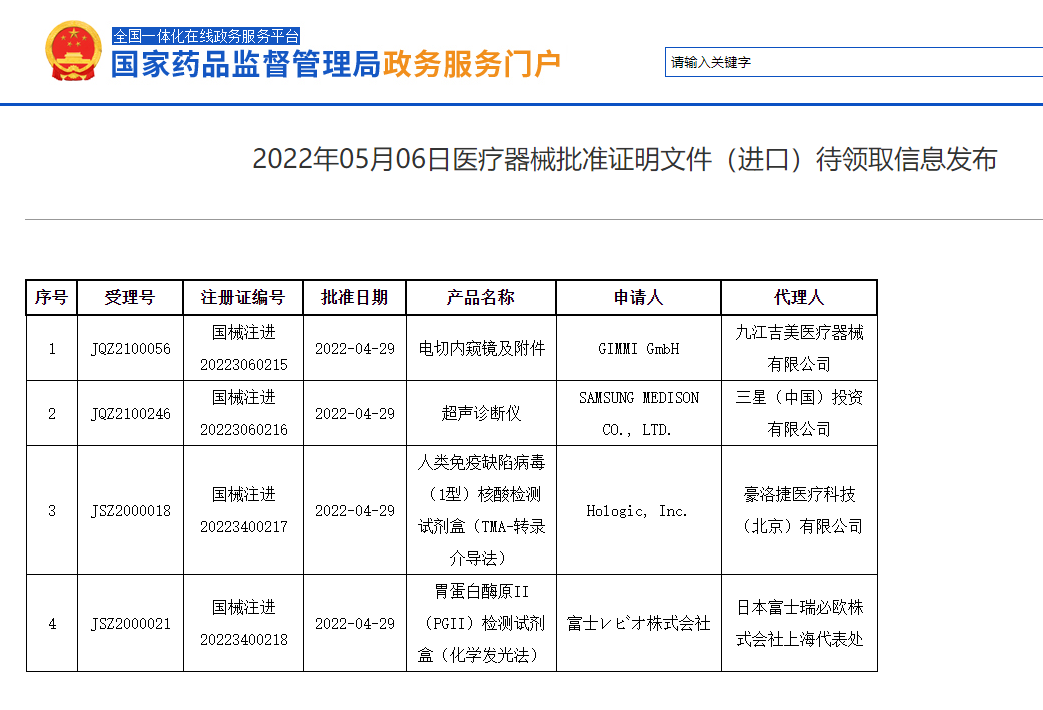
据悉,豪洛捷此次获批的Aptima®HIV核酸检测试剂盒是目前中国市场上唯一可同时进行定性和定量的检测试剂,适用于《中国艾滋病诊疗指南(2021年版)》中所有需要核酸诊断的场景。能够帮助实验室和医院更及时、快速、精准地提供诊断结果,为患者治疗带来更可靠的诊断依据。
Aptima®HIV核酸检测试剂盒既可作为HIV感染诊断的补充试验,用于急性期/窗口期以及晚期患者的诊断、HIV感染者的诊断和小于18月龄婴幼儿HIV感染的诊断,也可以用于预测疾病进程、评估抗逆转录病毒治疗(ART)疗效、指导ART方案调整。其样本类型包括血清和血浆,可以避免确诊实验室因不确定样本类型而导致样本无法检测的情形;灵敏度较高,检出限(LoD)低至12 拷贝/ml,对预测疾病进程、评估ART疗效、指导ART方案调整均能够提供帮助。
2021年6月,联合国大会曾表决通过关于到2030年结束艾滋病流行的宣言。承诺:2030年前实现“三个95%”目标,即95%的HIV感染者能得到确诊,95%的确诊者能获得抗逆转录病毒治疗(ART),以及95%的接受治疗者体内病毒得到抑制。而“扩大筛查和诊断面、提高ART治疗率”是实现目标的重要策略之一。
豪洛捷全球副总裁、豪洛捷中国集团总经理曹承治表示:“豪洛捷Aptima®HIV核酸检测试剂盒(RT-TMA法)的成功获批,以及Panther®全自动核酸检测系统解决方案的搭载,将为HIV的诊疗提供更加精准的结果,助力‘三个95%’目标的实现,为结束艾滋病流行和进一步实现健康中国的目标贡献力量。”
参考文献:
①中国艾滋病诊疗指南(2021年版)[J].协和医学杂志,2022,13(2):203-226.
②Political Declaration on HIV and AIDS: Ending Inequalities and Getting on Track to End AIDS by2030.https://undocs.org/A/RES/75/284.Accessed(2021-09-20).
(责编:荆雪涛)












