(人民日报健康客户端记者 乔靖芳)又获批1个!3月11日,国家药品监督管理局应急审批通过广东和信健康科技有限公司新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金法)。
截至目前,获批上市的新冠病毒检测产品增至16个,其中新冠病毒核酸检测试剂10个,抗体检测试剂6个。
16个获批的快检产品中,这是第三个抗体检测试剂盒(胶体金法)。这种试剂盒能在患者感染第7天或发病第3天就检测出lgM抗体,IgM抗体阳性则表示近期感染。
近日,《新冠肺炎诊疗方案(试行第七版)》提到,“确诊病例在核酸测定的基础上增加了抗体检测”。核酸阳性只能代表有病毒,出现抗体则可以表明人体确实受到病毒感染,是对核酸检测的一个很好的补充,抗体相关指数变化,也是确诊的“金标准”。
不过,鉴于抗体检测试剂方法学特点,新获批的抗体检测试剂盒产品仅用作对新型冠状病毒核酸检测阴性疑似病例的补充检测指标或疑似病例诊断中与核酸检测协同使用,不作为新型冠状病毒感染的肺炎确诊和排除的依据,不适用于一般人群的筛查。仅限医疗机构使用。
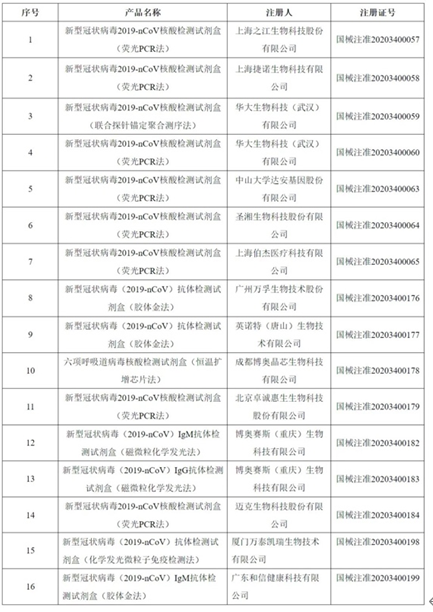
已批准新冠病毒检测试剂清单:












网友评论