( 实习记者 赵苑旨)“现在想起来还是很不可思议的工作,非常快速地把临床试验开展了。”中国工程院院士陈薇感叹到。
8月29日国家癌症中心结直肠癌国际高峰论坛上,陈薇院士在会上分享了疫苗研发过程和经历。而她所带队研发的重组新冠疫苗Ad5-nCoV是一种腺病毒重组疫苗,借助的是自有专利技术平台——腺病毒载体的基础平台,而这个技术平台早先也曾成功研制出埃博拉疫苗。
疫苗研发 走在世界前列
1月26日,陈薇受命率军事医学专家组赶赴武汉,围绕新型冠状病毒的病原传播变异、检测技术、疫苗抗体研制等展开研究。
3月16日,陈薇带领科研团队研制的新冠病毒疫苗,成为国内第一个获批正式进入临床试验的疫苗,第I期临床的108个人在注射疫苗后全部产生了抗体,健康状况良好。该试验结果发表在5月22日的《柳叶刀》上。试验结果表明:该疫苗安全、耐受性好,无严重不良反应,受试者全部产生抗体和细胞免疫反应,是一个重要的里程碑。

关于此次临床试验,陈薇谈到,3月16日晚上8点18分我们在武汉获批临床,并在当天晚上完成了第一个受试者的接种,比美国莫德纳公司mRNA 疫苗算下来要早5个半小时开展临床试验。
虽然疫苗的快速研发离不开国家绿色通道,但获批也离不开本身的研究的科学性和标准性。陈薇表示,在申请临床实验前,疫苗有效性已经历了恒河猴、雪貂、转基因hACE2小鼠试验及猴子大动物安全性的试验。
4月12日,该疫苗开展II期临床试验,率先进入II期随即、双盲、安慰剂对照临床试验,成为当时全球唯一进入二期临床试验的新冠病毒疫苗。这期临床试验陈薇院士团队重点关注了55岁以上年长人群,将508名受试者随机分配至疫苗组和安慰剂组,在更多人群中验证疫苗的安全性和免疫原性。试验结果表明,在单次接种该型重组新冠疫苗(腺病毒载体)28天后,99.5%的受试者产生了特异性抗体,89.0%的受试者产生了特异性细胞免疫反应,有望为人体对抗新冠病毒感染提供“双重保护反应”,同时首次验证了55岁以上年长人群的免疫效果。
目前,全球已有超过100多个团队在竞相研发新冠病毒疫苗。我国有6种疫苗进入临床研究,其中有3种疫苗即将进入临床3期试验。这期主要针对18岁以上人群中开展的适应性、随机、双盲、安慰剂对照的多中心III期临床试验,评价Ad5-nCoV单剂肌肉注射的有效性、安全性和免疫原性。
疫苗安全是第一位 用数据说话
“疫苗是给健康人用的,所以安全是第一位的。”陈薇院士近期在接受央视军事频道记者采访时谈到,作为普通药物来说,有效是放在第一位的,安全排在第二位,但是对于疫苗来说,安全则是需要放在第一位的。在陈薇团队的实验中,为了维护安全性,她们开始时,通常用最少的剂量,循序渐进,在确保安全的情况下,一点点增加剂量,来进行试验。
关于腺病毒重组疫苗副作用与安全性的问题,陈薇院士谈及,5月22日发表第一份报告时,大家说疫苗副作用大,发热率很高等等。但那是因为国内外发热标准不一致所致。目前在国外38℃以上才算发热,但国内37.3℃就算发热,如果按照美国标准38℃以上才算发热的,我们发热率只有4.8%。还有疲乏是37%,头痛是29.7%等,而注射部位的疼痛主要是一二级别的占54.5%。
“其实从疫苗数据汇总来看,我们现在做的病毒载体疫苗,比较而言还是比较安全的。”陈薇说。
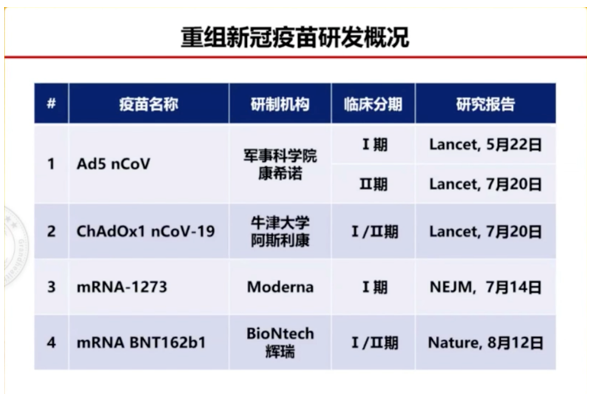
临床数据比较
陈薇院士表示,现在新冠疫苗是热点,大家关注度很高,也需要客观报道、慎重解读各种数据。
目前,重组新冠疫苗Ad5-nCoV的III期临床试验也在推进中。陈薇说:“我们现在做了4万人的全球临床方案,正在多个国家正在推进,包括俄罗斯、巴基斯坦、沙特等。全世界大家都在共同努力做。”
(责编:李宁)












